Cuando nuestro médico nos receta un fármaco, le acompaña un impreso cuidadosamente doblado en el que se describen las propiedades del fármaco, sus indicaciones, la forma en que debe tomarse y sus efectos secundarios posibles.
Debemos saber que antes que este fármaco haya llegado a nuestras manos, ha seguido un largo camino. La intención de este mi primer artículo es mostrarles (espero que sea amena) este largo camino seguido y las regulaciones que obligan a que éste sea eficaz y seguro.
En la hora de mi ya inminente jubilación quiero compartir lo que ha sido mi vida profesional en los últimos 30 años, la Investigación Clínica en fármacos y productos sanitarios. También el objetivo de este artículo será darles información desde otro lado para que puedan contrastar y formarse una opinión propia.
Estos sería ejemplos de noticias en periódicos de tirada nacional en los que se habla con poco conocimiento de la Investigación Clínica.
DEL LABORATORIO A LA FARMACIA:
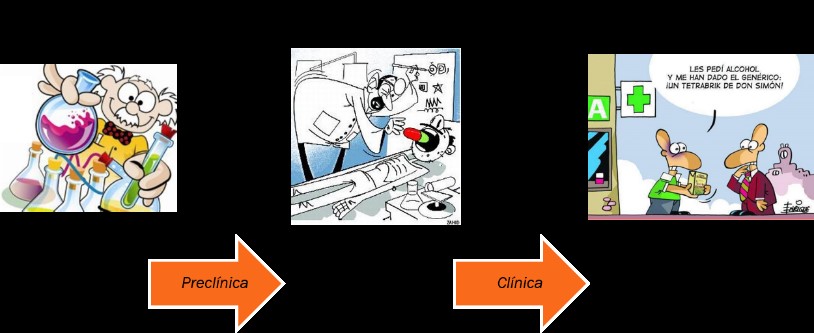
Los medicamentos que se nos prescriben cuando enfermamos, siguen un largo camino desde el momento en que un investigador o grupo de investigadores descubre una molécula, hasta que se aprueba para el consumo humano por las autoridades sanitarias.
El Laboratorio: El primer paso viene del conocimiento de un proceso físico o metabólico tanto en su faceta de funcionamiento normal como patológico, es decir la enfermedad. La identificación de que está alterado puede hacer que se pueda corregir desde “fuera”. Es decir, diseñar un fármaco. En esta fase intervienen médicos, biólogos, bioquímicos.
El segundo paso es ver los procesos para sintetizar esa molécula y el tercer paso es ver como esta molécula puede entrar en el interior del organismo para que haga el efecto terapéutico deseado. A eso le llamamos “galénica” y es la forma galénica de presentación del fármaco para su aplicación: comprimidos, cápsulas, pomadas, aerosoles, inyecciones…
Hay que clarificar en este punto que “entrar” en el organismo significa entrar en el torrente circulatorio. Para que este fármaco sea eficaz deberá tener unos determinados niveles o concentraciones plasmáticas.
La fase Preclínica: Una vez se ha identificado la molécula, se ha descrito como se sintetiza y se ha encontrado la forma galénica más adecuada para que haga el efecto deseado, llega el momento de que ese fármaco sea ensayado en organismos vivos. En este estadío el fármaco es testado en modelos animales: ratones, perros y monos. En este estadío se estudian principalmente:
- Los procesos a los que un fármaco es sometido a través de su paso por el organismo y trata de dilucidar qué sucede con un fármaco desde el momento en el que es administrado hasta su total eliminación del cuerpo. La Farmacocinética.
- Los efectos bioquímicos y fisiológicos de los fármacos y de sus mecanismos de acción y la relación entre la concentración del fármaco y el efecto de este sobre un organismo. La Farmacodinamia.
La fase Clínica:
Se refiere a cualquier experimento en el cual uno o más sujetos humanos reciben una medicina con el propósito de determinar la seguridad y la eficacia de un diagnóstico, la terapéutica o uso preventivo en sujetos humanos. Efectivamente es el inicio de la experimentación del fármaco en humanos paso último e indispensable para que las autoridades reguladoras: La Food and Drug Administration – FDA en EE. UU, la Agencia Europea de Medicamentos – EMA que agrupa a las diferentes agencias estatales como por ejemplo la Agencia Española de Medicamentos y Productos Sanitarios – AEMPS aprueben el fármaco después de valorar todo el inmenso dossier de investigación y autoricen su comercialización.
En la investigación en la fase clínica tiene distinguen 4 fases:
- Fase I: Se mide la seguridad y la eficacia. Es la primera vez que el fármaco se aplica en humanos. Normalmente son voluntarios sanos en los que se aplica el fármaco en dosis subclínicas. Esta fase de la experimentación se realiza en grupos pequeños (20-80 voluntarios).
- Fase II: Se define la dosis y la efectividad. Se realiza en ambientes hospitalarios y en pacientes con una determinada patología susceptible de ser tratada con el fármaco de investigación. Se realiza en grupos mayores de unos cientos de pacientes. En este tipo de estudios, se testa el fármaco administrado aleatoriamente a doble ciego frente a un comparador que puede ser el fármaco de referencia actual o placebo.
- Fase III: Se evalúa la seguridad y la eficacia. También se realiza en ambiente hospitalario también en pacientes con la patología interesada en el fármaco de estudio. Se realiza en grupos mayores de entre 1000 y unos 3000 pacientes. En este tipo de estudios, también testa el fármaco administrado aleatoriamente a doble ciego frente a un comparador que puede ser el fármaco de referencia actual o placebo.
- Fase IV: Se evalúa la seguridad en grupos más grandes. También realizada en ambiente hospitalario, los pacientes estudiados en este tipo de ensayos clínicos se cifran en miles. En este tipo de estudios, todos los pacientes incluidos reciben el fármaco en investigación en abierto.
Entre los trabajos de laboratorio, pasando por la fase de preclínica (experimentación en modelos animales hasta la finalización de la fase clínica suelen pasar entre 7 y 10 años.
La patente de una molécula convertida en fármaco tiene una validez de 15 años. A partir de ese momento cualquier laboratorio puede fabricarla libremente debiendo solamente demostrar ante las autoridades reguladoras bioequivalencia frente a la molécula original. Son los llamados genéricos.
Es importante reseñar que se estima que, de 10.000 moléculas descubiertas y sintetizadas, solo una llega al mercado. El resto, esas 9.999, pueden “caer” en las distintas fases por diversos motivos.
- Principalmente si no demuestran eficacia o su eficacia no es mayor que la del fármaco comparador con un coste más elevado (razones fármaco-económicas).
- Porque los efectos adversos son intolerables para la patología que van a tratar (seguridad y valoración riesgo-beneficio).
- Porque la vía de administración es inaceptable para la patología a tratar (no sería aceptable por ejemplo que para tratar una patología leve el fármaco se administre por un catéter en una vía central).
- Por dificultades en la síntesis
- Otras razones…
Como conclusión, me atrevería a decir que:
- El advenimiento de la Investigación Clínica controlada nos ha dado una herramienta con la cual, podemos, con confianza, proporcionar a los pacientes tratamientos que han probado ser seguros y efectivos.
- Los métodos que se usan para hacer estos estudios seguros y confiables deben su validez a los análisis bioestadísticos.








2 comentarios en «La investigación clínica: el largo camino de un fármaco (I) | Albert Mesa Rey»
Estupendo artículo, muy bien documentado y muy bien expuesto, delata la larga y experimentada trayectoria profesional de quien lo escribe así como sus amplios conocimientos en la materia. Enhorabuena Albert.
Muchas garcias por tus comentarios Enrique. Los ensayos clínicos has sido mi vida peofesional los últimos 30 años. Ha sido mi pequeñísima colaboración al desarrollo a las ciencias biomédicas, buscando que estuvieran disponibles medicamentos eficaces y seguros.
Un saludo.
Albert